Introdução
A hemodiafiltração (HDF) tem se consolidado como uma estratégia dialítica avançada, e de alta qualidade, combinando os princípios de difusão, assim como na hemodiálise convencional e convecção (arraste de moléculas) para ampliar a depuração de moléculas maiores.
Estudos observacionais e ensaios clínicos, como o Estudo Catalão ESHOL e o Trail randomizado CONVINCE, sugerem benefício clínico quando volumes convectivos elevados são alcançados com segurança.
Para todos os profissionais da saúde, compreender os parâmetros que levam as boas práticas de HDF é fundamental para garantir eficiência dialítica, com segurança ao paciente e estabilidade hemodinâmica.
Este artigo tem como objetivo, apresentar um modelo prático e técnico dos principais parâmetros que impactam o desempenho da HDF na rotina clínica.
Fundamentos da Hemodiafiltração
A HDF combina duas modalidades de terapia dialitica em uma, utilizando a difusão, para a remoção de pequenas moléculas como ureia, creatinina e a convecção, que realiza aremoção de moléculas médias como β2-microglobulina e citocinas.
O mecanismo convectivo, da terapia, depende diretamente do volume de substituição infundido, que está relacionado ao fluxo sanguíneo efetivo e ao tempo de sessão.
1. Fluxo Sanguíneo (Qb): Fator principal
A Recomendação prática é de fluxos ≥ 350–400 mL/min, para uma boa convecção, porém o mínimo aceitável para HDF de alto volume: ≥ 300 mL/min. O volume convectivo possível é diretamente proporcional ao Qb real. Qb baixo limita varios fatores da terapia como:
- Fração de filtração
- Volume de substituição
- Depuração de moléculas médias
Os profissionais ligados a realização da terapia, devem ficar atentos as condições que possam impactar no resultado da terapia. Sempre devem observar e intervir:
✔ Avaliar funcionalidade do acesso vascular
✔ Monitorar pressões arterial e venosa
✔ Identificar sinais precoces de recirculação
2. Tempo de Sessão
O tempo de sessão, também tem impacto direto no volume de convecção. A recomendação prática, para atingir volumes convectivos altos é de 4 horas ou mais. Sessões curtas reduzem a possibilidade de atingir volume convectivo alvo.
O volume convectivo total depende da equação simplificada:
Volume convectivo total ≈ Fluxo de substituição + UF clínica × Tempo
Assim, mesmo com Qb adequado, sessões reduzidas podem comprometer substancialmente o desempenho esperado na terapia.
3. Volume Convectivo Total: O Principal Marcador de Qualidade
Diversos estudos validados apontam que volumes convectivos elevados estão associados a melhores desfechos. Para isso a meta observada nestes e recomendada é ≥ 23 litros por sessão (pós-dilucional). Estes estudos demonstram redução de mortalidade em pacientes que atingiram volumes elevados reforçando a importância da HDF de alto volume com segurança operacional.
Para que o volume convectivo seja atingido, é necessário que alguns critérios sejam atingidos como:
- Qb adequado
- Controle da fração de filtração
- Monitorização constante de pressões transmembrana
4. Fração de Filtração (FF)
Observar a fração de filtração é mais do que apenas ver um número na terapia, ela é responsável por manter a estabilidade de pressões do sistema de sangue até o final da sessão. Para que essa estabilidade se mantenha, o valor ideal da FF deve ficar entre 20 e 25%, Valores acima de 30% aumentam risco de:
- Hemoconcentração
- Coagulação do sistema
- Elevação da pressão transmembrana
É fundamental que o profissional de saúde monitore:
- Tendência de aumento progressivo da TMP
- Formação de coágulos no filtro
- Necessidade crescente de intervenções, para correção de volume de substituição ou de sangue no equipamento
5. Volume convectivo Total
Na HDF, o volume convectivo total é composto pelas UF clínica (remoção de volume do paciente) e UF adicional convectiva (volume de substituição)
Fórmula simplificada:
Volume Convectivo Total = UF clínica + UF adicional convectiva
Exemplo:
Um paciente com uma UF clínica de 2,5 L, com uma prescrição de substituição de 23 L, leva a realização de uma UF adicional convectiva igualmente ao valor de substituição 23 L, logo o valor de UF total do sistema será de 25,5 L, a esse valor chamamos de Volume Convectivo total. Esse volume elevado exige estabilidade hemodinâmica e de fluxos adequada.
6. Estabilidade Hemodinâmica
HDF de alto volume pode melhorar tolerância hemodinâmica quando bem conduzida, mas como toda terapia extracorpórea tem seus riscos e estes incluem:
- Hipotensão intradialítica
- Cãibras
- Sintomas autonômicos
- Hipoglicemia
- Alcalose
- Hipocalemia
Estratégias práticas
✔ Ajuste individualizado da taxa de UF, buscando uma retirada controlada do peso do paciente
✔ Controle de temperatura do dialisato, como estratégia de manutenção da PAS
✔ Avaliação de peso seco, pois esses pacientes têm tendencia a melhora de alimentação e consequente ganho de massa muscular
✔ Realizar uso de soluções de fração acida com glicose
✔Acompanhar a concentração de Bicarbonato pré dialise do meio da semana em pacientes com introdução recente na terapia
✔ Acompanhar a concentração de Potássio pré dialise do meio da semana em pacientes com introdução recente na terapia
✔ Comunicação ativa com o paciente para identificação de quaisquer alteração ou sintomas
7. Anticoagulação Eficaz
A anticoagulação deve ser suficiente para prevenir coagulação extracorpórea, sem aumentar risco hemorrágico. Podendo utilizar:
- Heparina não fracionada
- Heparinas de baixo peso molecular
A escolha depende de:
- Protocolo institucional
- Risco hemorrágico
- Perfil do paciente
Monitorar:
- Formação de fibrina
- Coagulação parcial do circuito
Organograma Integrado da HDF
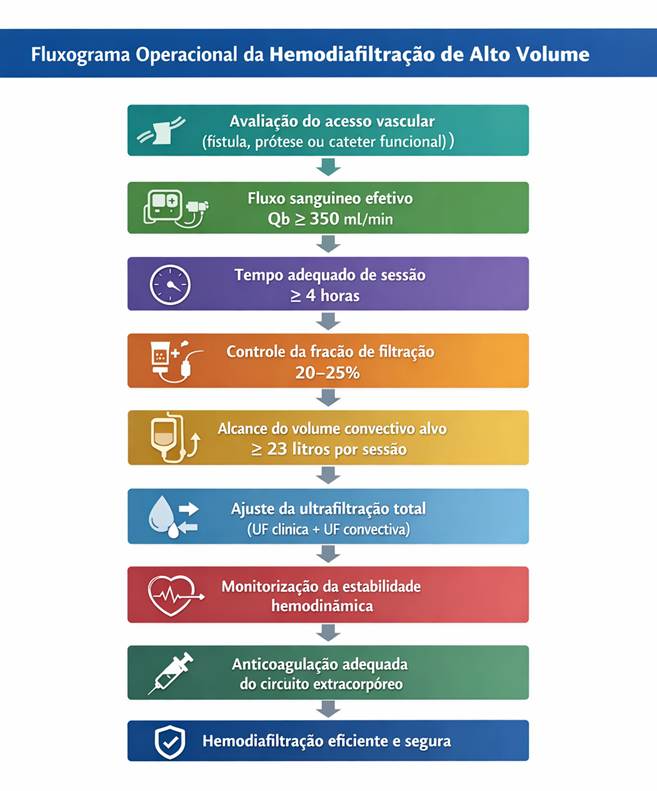
Gráfico Conceitual: Relação entre Qb e Volume Convectivo
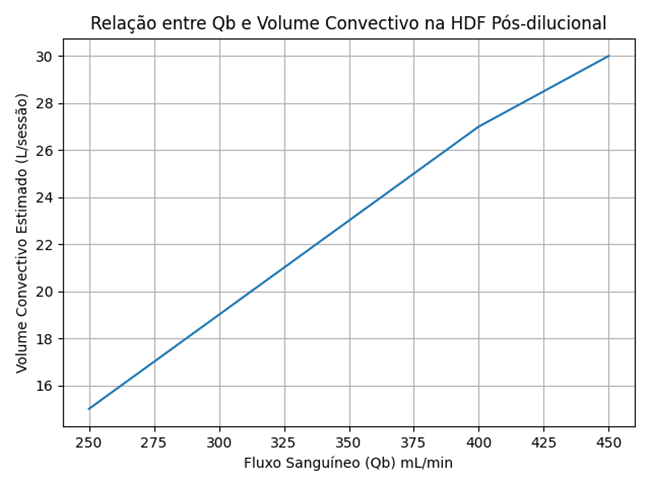
Quanto maior o Qb real sustentado, maior o potencial de volume convectivo atingível.
Checklist Prático para Equipe de Saúde
Antes da sessão
☐ Avaliar acesso vascular
☐ Conferir prescrição
☐ Checar anticoagulação
☐ Definir meta de volume convectivo
Durante a sessão
☐ Monitorar TMP
☐ Observar sinais de coagulação
☐ Avaliar estabilidade hemodinâmica
☐ Confirmar volume convectivo acumulado
Após a sessão
☐ Confirmar volume final alcançado
☐ Registrar intercorrências
☐ Avaliar adequação dialítica
Pontos Críticos e Limitações
Nem todos os pacientes são candidatos ideais à HDF de alto volume, assim como qualquer tipo de tratamento, é fundamental a individualização da terapia ofertada. Existem limitações para a indicação do paciente a terapia e estão ligadas a acesso vascular inadequado com fluxos baixos, instabilidade hemodinâmica recorrente, distúrbios de coagulação diversos, baixa adesão ao tempo de sessão total por sessão e intolerância a altos fluxos de sangue (Qb). A individualização é mandatória e é responsável pelo sucesso da terapia.
Hemodiafiltração Pré-dilucional: Quando Utilizar?
A hemodiafiltração pode ser realizada em duas modalidades principais:
- Pós-dilucional (mais utilizada no Brasil e no mundo)
- Pré-dilucional
Na modalidade pré-dilucional, o fluido de substituição é infundido antes do filtro (antes do dialisador), promovendo diluição do sangue antes da passagem pela membrana, reduzindo assim o risco de hemoconcentração e a eficácia da terapia, com o mesmo volume de substituição.
Indicações Clínicas da HDF Pré-dilucional
A pré-diluição é especialmente considerada quando há:
1. Fluxo sanguíneo é limitado
- Qb < 300 mL/min
- Acesso vascular de baixa performance
- Fístulas com tendência a colabamento
2. Alto risco de coagulação do sistema
- Hematócrito elevado
- Hiperviscosidade
- Tendência à elevação da PTM por impossibilidade de uso de anticoagulante
3. Instabilidade hemodinâmica
- Pacientes com hipotensão frequente em uso da HDF pós dilucional
- Idosos frágeis sem tolerância a altos fluxos de Qb
- Cardiopatas avançados, com alteração hemodinâmica em terapia
4. Cenários técnicos específicos
- Em protocolos japoneses seu uso amplamente difundido, devido ao uso de fluxos de sangue baixos
- Unidades com política de segurança voltada à redução de hemoconcentração
Aspectos Técnicos da HDF Pré-dilucional
Na terapia HDF com substituição pré-diluição o sangue é diluído antes da filtração, isso leva a hemoconcentração intradialisador reduzida e assim a fração de filtração pode ser maior sem risco imediato de coagulação. Contudo, ocorre um efeito importante:
A diluição prévia reduz a concentração de solutos no plasma que chega à membrana, diminuindo a eficiência convectiva por litro infundido.
Isso significa que, para alcançar eficácia semelhante à pós-diluição, são necessários volumes convectivos significativamente maiores.
Comparação Técnica: Pós vs Pré-diluição
| Parâmetro | Pós-diluição | Pré-diluição |
| Local de infusão da substituição | Após o filtro | Antes do filtro |
| Eficiência por litro | Alta | Menor |
| Risco de hemoconcentração | Maior | Menor |
| Risco de coagulação | Maior | Reduzido |
| Volume necessário para mesma eficácia | ≅ 23L | 1,5 a 2 vezes maior |
| Indicação preferencial | Qb elevado | Qb baixo / risco de coagulação |
Volume Convectivo na Pré-diluição
Enquanto na pós-diluição a meta é ≥ 23 L por sessão, na pré-diluição para alcançar depuração semelhante, frequentemente são necessários volumes que chegam a valores de 40 a 50 L por sessão.
Essa diferença ocorre pela diluição plasmática antes da filtração, estudos do grupo europeu de diálise (EUDIAL) e análises fisiológicas demonstram essa necessidade de ajuste volumétrico, para alcance do mesmo benefício clínico, quando comparamos as terapias.
Benefícios da HDF Pré-dilucional
✔ Redução significativa da hemoconcentração
✔ Menor elevação da pressão transmembrana
✔ Menor risco de coagulação do sistema
✔ Maior tolerância em pacientes instáveis
✔ Permite uso mesmo com Qb menores
Para a enfermagem, isso se traduz em:
- Menor necessidade de intervenções por coagulação
- Menor troca precoce de filtro
- Maior estabilidade do circuito
Limitações da HDF Pré-dilucional
- Menor eficiência por litro infundido
- Necessidade de volumes convectivos maiores
- Maior consumo de fluido de substituição
- Pode demandar tempo de sessão maior
- Benefício clínico em mortalidade menos consistente que na pós-diluição de alto volume
Os grandes ensaios clínicos de impacto em mortalidade, como o Estudo ESHOL e o Trial Randomizado CONVINCE, foram conduzidos predominantemente com pós-diluição de alto volume, o que reforça sua posição como padrão preferencial quando tecnicamente possível.
Considerações Práticas para a Equipe de Saúde
Em HDF Pós-dilucional:
- Monitorar TMP de forma rigorosa
- Avaliar sinais de hemoconcentração
- Ajustar fração de filtração sempre que necessário
Em HDF Pré-dilucional:
- Monitorar volume total infundido
- Garantir adequação do tempo de sessão para atingir todo o volume convectivo
- Avaliar eficiência dialítica global (Kt/V, redução de β2-microglobulina)
Conclusão
A hemodiafiltração on-line representa uma evolução técnica relevante na terapia renal substitutiva. No entanto, seu benefício clínico depende da execução adequada dos parâmetros operacionais.
Para enfermeiros, residentes e técnicos de enfermagem, compreender a relação entre: Fluxo sanguíneo, tempo de sessão, fração de filtração, volume convectivo, ultrafiltração total, estabilidade hemodinâmica e anticoagulação, é determinante para transformar prescrição em resultado clínico real.
A HDF pré-dilucional pode ser uma alternativa valiosa em cenários de limitação técnica ou risco aumentado de coagulação, ampliando a aplicabilidade da terapia.
A escolha não deve ser dogmática, mas baseada em:
- Perfil clínico do paciente
- Condições do acesso vascular
- Capacidade operacional da unidade
- Monitorização adequada da equipe
A excelência na HDF não depende apenas da tecnologia, mas da capacidade crítica da equipe em ajustar parâmetros à realidade clínica.
Referências Bibliográficas
- Maduell F, Moreso F, Pons M, Ramos R, Mora-Macía J, Carreras J, et al. High-efficiency postdilution online hemodiafiltration reduces all-cause mortality in hemodialysis patients. J Am Soc Nephrol. 2013;24(3):487–97.
- Blankestijn PJ, Fischer KI, Barth C, Canaud B, Davenport A, Grooteman MPC, et al. Effect of online hemodiafiltration on all-cause mortality and cardiovascular outcomes: results of the CONVINCE randomized clinical trial. N Engl J Med. 2023;389:1469–79.
- Grooteman MPC, van den Dorpel MA, Bots ML, Penne EL, van der Weerd NC, Mazairac AH, et al. Effect of online hemodiafiltration on all-cause mortality and cardiovascular outcomes. J Am Soc Nephrol. 2012;23(6):1087–96.
- Ok E, Asci G, Toz H, Ok ES, Kircelli F, Yilmaz M, et al. Mortality and cardiovascular events in online haemodiafiltration (Turkish OL-HDF Study). Nephrol Dial Transplant. 2013;28(1):192–202.
- Tattersall J, Ward RA; EUDIAL Group. Online haemodiafiltration: definition, dose quantification and safety revisited. Nephrol Dial Transplant. 2013;28(3):542–50.
- Canaud B, Bragg-Gresham JL, Marshall MR, Desmeules S, Gillespie BW, Depner T, et al. Mortality risk for patients receiving hemodiafiltration versus hemodialysis. Kidney Int. 2006;69(11):2087–93.
- Masakane I, Sakurai K. Current approaches to hemodiafiltration in Japan. Contrib Nephrol. 2011;168:134–43.
- Davenport A. Practical guidance for dialysate substitution fluid volumes in pre- and post-dilution haemodiafiltration. Hemodial Int. 2015;19 Suppl 1:S30–5.
- Kidney Disease: Improving Global Outcomes (KDIGO) Work Group. KDIGO clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney Int Suppl. 2013;3(1):1–150.